- 股票掌故
- 香港股票資訊
- 神州股票資訊
- 台股資訊
- 博客好文
- 文庫舊文
- 香港股票資訊
- 第一財經
- 微信公眾號
- Webb哥點將錄
- 港股專區
- 股海挪亞方舟
- 動漫遊戲音樂
- 好歌
- 動漫綜合
- RealBlog
- 測試
- 強國
- 潮流潮物 [Fashion board]
- 龍鳳大茶樓
- 文章保管庫
- 財經人物
- 智慧
- 世界之大,無奇不有
- 創業
- 股壇維基研發區
- 英文
- 財經書籍
- 期權期指輪天地
- 郊遊遠足
- 站務
- 飲食
- 國際經濟
- 上市公司新聞
- 美股專區
- 書藉及文章分享區
- 娛樂廣場
- 波馬風雲
- 政治民生區
- 財經專業機構
- 識飲色食
- 即市討論區
- 股票專業討論區
- 全球政治經濟社會區
- 建築
- I.T.
- 馬後砲膠區之圖表
- 打工仔
- 蘋果專欄
- 雨傘革命
- Louis 先生投資時事分享區
- 地產
Random Tags
和黃中國醫藥科技專區
1 : GS(14)@2019-04-18 07:47:56https://www.hmplglobal.com/cn/
关于我们
和记黄埔医药(上海)有限公司隶属于和黄中国医药科技有限公司(Chi-Med),专注于研发针对癌症和自身免疫性疾病的靶向药物,致力于成为全球创新药研发领导者。
和黄中国医药科技有限公司(Chi-Med)在英国AIM证券交易所和美国纳斯达克上市,股票代号为HCM。
在研新药
公司自主研发的抗肿瘤及免疫系统的创新药物产品管线丰富,多项临床研究正在北美,欧洲,中国及澳大利亚全面开展。
最新信息
2019年03月29号
和记黄埔医药在中国启动索凡替尼以不可切除或转移性胆道癌为适应症的IIb/III期临床试验
2019年03月28号
和记黄埔医药将于AACR年会上以口头报告形式公布沃利替尼肺癌相关项目进展
2019年02月12号
沃利替尼/Imfinzi®联合疗法以治疗晚期乳头状肾细胞癌为适应症的II临床研究初步数据将于2019年ASCO泌尿生殖系统肿瘤研讨会发表
http://www.hutchison-whampoa.com/tc/businesses/others.php
和黃附屬公司和黃中國醫藥科技是一家從事醫藥與保健業務集團的控股公司,主要以中國內地為基地,在倫敦證券交易所另類投資市場上市(股份代號:HCM)。和黃中國醫藥科技專門從事研究、開發、製造與銷售藥物及以保健為主的消費產品。
https://www.chi-med.com/
website
2 : GS(14)@2019-04-18 07:48:23
https://www.hmplglobal.com/cn/%E ... %E4%BA%A7%E5%93%81/
和记黄埔医药专注研发治疗癌症和自身免疫性疾病的创新药物。公司拥有多个在研产品,其中数个候选药物有可能成为全球同类疗法中的首创,而其他候选药物与已获批的针对相关激酶靶点的药物相比具有良好的药物特性及差异性,因此有潜力成为全球同类最佳的下一代靶向药物。我们的候选药物正在多种适应症中展开研究。
关于最新的研究进展,请点击公司新闻、学术发布或我们母公司Chi-Med (AIM/NASDAQ: HCM) 的最新公司报道页面查看。
(截至2019年1月07日)
注:概念验证 = Ib/II期临床研究;AML = 急性髓系白血病;CLL/SLL = 慢性淋巴细胞白血病 / 小淋巴细胞淋巴瘤;CSF-1R = 集落刺激因子-1受体;c-MET = 间充质上皮转化因子;DLBCL = 弥漫性大B细胞淋巴瘤;EGFR = 表皮生长因子受体;EGFRm = EGFR突变;EGFR wt = EGFR野生型;FGFR = 成纤维细胞生长因子受体;FL = 滤泡型淋巴瘤;ITP = 特发性血小板减少性紫癫;MCL = 套细胞淋巴瘤;MET+ = MET扩增;MZL = 边缘区淋巴瘤;NHL = 非霍奇金淋巴瘤;PD-1 = 程序性细胞死亡蛋白-1;PD-L1 = 程序性细胞死亡蛋白-1配体;PI3Kδ = 磷酸肌醇3′-激酶亚型δ;Syk = 脾酪氨酸激酶;TKI= 酪氨酸激酶抑制剂;VEGFR = 血管内皮生长因子受体;WM = 华氏巨球蛋白血症;全球 = 超过2个国家。
沃利替尼 (AZD6094/HMPL-504 )
沃利替尼是一种有潜力成为全球首创的间充质上皮转化因子(c-MET)受体酪氨酸激酶抑制剂,c-MET已被证明在多种实体瘤中表现异常。 沃利替尼是一种高选择性的口服抑制剂,通过化学结构的优化来解决肾毒性的问题,而肾毒性是所有其他选择性c-MET抑制剂未能获批的主要原因。 在我们的临床研究中,沃利替尼未显示出肾毒性,并且在c-MET基因扩增的乳头状肾细胞癌,非小细胞肺癌,结直肠癌和胃癌患者中观察到了肿瘤缩小,显示出了较好的疗效。
我们目前正与阿斯利康合作,在多个平行研究中检测沃利替尼作为单一疗法,以及联合其他靶向疗法和化疗时的疗效。
呋喹替尼 (HMPL-013)
呋喹替尼是一种高选择性的血管内皮生长因子受体(VEGFR)口服抑制剂,我们认为它有潜力成为全球同类最佳的能够治疗多种实体瘤的VEGFR抑制剂。根据迄今为止的临床前和临床研究资料,呋喹替尼的激酶选择性被证实能够降低脱靶毒性。该条件下药物暴露量可以完全抑制VEGFR,且有潜能可以在接受早期治疗的更大的患者群体中与其他靶向疗法和化疗联合使用(VEGFR是一种有助于肿瘤周围新生血管生成的受体酪氨酸激酶,从而有助于肿瘤增长)。高效、低毒、适合联合用药是呋喹替尼区别于其他已获批的小分子VEGFR抑制剂的优良特性。
和记黄埔医药目前正与合作伙伴礼来联手在中国开展呋喹替尼治疗结直肠癌,非小细胞肺癌和胃癌的各项研究。此外,我们在苏州设立了工厂,并配备了一整套制剂生产设施,负责生产供应呋喹替尼胶囊。
索凡替尼 (HMPL-012)
索凡替尼是一种可选择性抑制与血管内皮生长因子受体(VEGFR)和成纤维细胞生长因子受体1(FGFR1)相关的酪氨酸激酶活性及集落刺激因子-1受体(CSF-1R)的口服候选药物,成纤维细胞生长因子受体1(FGFR1)是肿瘤增长中起作用的蛋白质的受体, 而集落刺激因子-1受体(CSF-1R)参与阻断肿瘤相关巨噬细胞活化的信号通路,它能庇护癌细胞免受T细胞的杀伤性攻击。
目前,我们正在数个疾病领域(如胰腺和非胰腺神经内分泌肿瘤和胆管癌)开展多项临床试验,并保留索凡替尼在全球的所有权利。 索凡替尼是和记黄埔医药自主完成在中国的概念验证试验,并扩展到美国进行临床研究的第一个肿瘤候选药物。
依吡替尼 (HMPL-813)
相当一部分的非小细胞肺癌患者会进展至脑转移。 脑转移患者的预后不良,中位总生存期少于6个月,而且生活质量低下,治疗方案的选择有限。依吡替尼是一种高效及高选择性的表皮生长因子受体(EGFR)口服抑制剂,已经在临床前和临床研究中证明了脑渗透及其功效。用于治疗EGFR激活突变的非小细胞肺癌的各种EGFR抑制剂开发取得了革命性的进展, 然而,已获批的EGFR抑制剂如吉非替尼和厄洛替尼无法有效地渗透血脑屏障,使得许多脑转移患者陷入缺乏有效靶向治疗的困境。 我们目前保留依吡替尼在全球范围内的所有权利。
西利替尼 (HMPL-309)
像依吡替尼一样,西利替尼是一种新型分子表皮生长因子受体(EGFR)抑制剂,现正用于治疗各种实体瘤的临床研究中。 具有野生型EGFR激活的肿瘤,例如通过基因扩增或蛋白质过表达,因其次佳的反应亲和力,对目前的EGFR酪氨酸激酶抑制剂吉非替尼和厄洛替尼的敏感度较低。西利替尼被设计成对野生型EGFR激酶具有很强的亲和力,在研究中证实有效性比厄洛替尼高五到十倍。 因此,我们认为,西利替尼可以使具有野生型EGFR激活高发生率的食管癌和头颈癌的患者受益。我们目前保留西利替尼在全球范围内的所有权利。
HMPL-523
HMPL-523有潜力成为全球首创的靶向脾酪氨酸激酶(Syk)的口服抑制剂,其靶点Syk是B细胞信号传导通路中的一个关键蛋白。 B细胞信号传导系统的调节被证实可用于某些慢性免疫疾病的治疗,如类风湿性关节炎以及血液肿瘤。截至目前,只有使用患者自身免疫系统治疗疾病的单克隆抗体免疫调节剂已经获批。作为一种口服候选药物, HMPL-523在类风湿性关节炎中具有优于单克隆抗体免疫调节剂的重要优势,因为小分子化合物可以更快地从机体中清除,从而降低由于持续抑制免疫系统而受到的感染风险。
此外,其他医药研发公司也在尝试设计用于治疗慢性免疫疾病的小分子Syk抑制剂,但激酶选择性不佳容易产生脱靶毒性,比如高血压,所以成功地设计出一款针对主流慢性疾病的有效且安全的Syk抑制剂困难重重。 HMPL-523克服了脱靶毒性的问题,是一种强效且高选择性的口服抑制剂。Syk抑制剂一旦开发成功,其市场潜力巨大。我们目前保留HMPL-523在全球范围内的所有权利。
HMPL-689
HMPL-689是一种靶向磷酸肌醇3′-激酶亚型δ(PI3Kδ)的新型高选择性小分子抑制剂,PI3Kδ是B细胞受体信号通路中的一个关键组成部分。HMPL-689具有专门针对PI3Kδ靶点优异的选择性,特别是不抑制同族另一亚型PI3Kɣ(γ)的活性,可以最大限度地减少由免疫抑制引起严重感染的风险。 HMPL-689具有很强的药效,特别是在全血水平下活性仍然很高,方便低剂量使用,从而避免产生与化合物相关的毒性,如在已获批的第一代PI3Kδ抑制剂中观察到的高水平的肝毒性。临床前药代动力学研究证实HMPL-689具有良好的口服吸收率,中等的组织分布和低清除率。临床前研究还预测HMPL-689的药物蓄积以及药物与药物相互作用的风险较低。因此,我们认为HMPL-689有潜力成为全球同类最佳的PI3Kδ药物。我们目前保留HMPL-689在全球范围内的所有权利。
HMPL-453
HMPL-453是靶向成纤维细胞生长因子受体(FGFR)1/2/3(受体酪氨酸激酶亚族)的新型高选择性小分子候选药物。 经研究发现异常的FGFR信号传导是肿瘤增长(通过组织生长和修复),促进肿瘤血管生成和对肿瘤治疗产生抗性的驱动因子。 目前,还没有专门针对FGFR信号通路的获批疗法。 在临床前研究中,与同类其它候选药物相比,HMPL-453显示出了良好的激酶选择性、安全性和抗肿瘤药效。我们目前保留全球HMPL-453在全球范围内的所有权利。
3 : GS(14)@2019-04-18 07:48:52
https://zh.wikipedia.org/wiki/%E ... 2%E7%A7%91%E6%8A%80
和記中國醫療科技
維基百科,自由的百科全書
跳至導覽跳至搜尋
和黃中國醫療科技有限公司,簡稱和黃中國醫療科技(英語:HUTCHISON CHINA MEDITECH LIMITED,LSE:HCM、NASDAQ:HCM),於2000年由和記黃埔有限公司分拆成立。
主席為杜志強,首席執行官為Christian Hogg,而主要業務於中國內地經營生產及銷售各種中成藥產品[1],總部位於香港金鐘夏慤道10號和記大廈22樓。
而在2006年4月初,也就是復活節時期,和記黃埔把旗下本公司分拆至倫敦證券交易所另類投資市場上市[2],則在2006年5月19日上市,當時招股價為2.75英鎊,集資額為4000萬英鎊[3]。
2015年10月16日,該公司正計劃向美國證交會申請第1表格於納斯達克(以美國存託憑證)上市[4]。
4 : GS(14)@2019-04-18 07:49:04
https://inews.hket.com/article/2 ... %82%A160-?mtc=20023
和黃中國醫藥科技申請主板上市 長和持股60%
金融經濟 14:21 2019/04/15
分享:
長和(00001)持股60.2%的創新生物製藥公司「和黃中國醫藥科技」,周一提交主板上市申請。申請文件顯示,公司去年收入為2.14億元(美元,下同),按年跌11%;應佔虧損為7,481萬元,按年擴大近5,000萬美元。
和黃中國醫藥科技主席杜志強表示,很高興宣布集團在港申請上市的消息,特別是港交所去年放寬生物科技公司上市的上市規則,認為現時在港尋求上市可帶來莫大脾益。若可以成功上市,預期可以加強集團的藥物研發能力,繼續發展成國際性的生物製藥公司。
和黃中國醫藥科技主席杜志強(網頁截圖)
▲ 和黃中國醫藥科技主席杜志強(網頁截圖)
雖然所發行的新股尚未定案,但和黃中國醫藥預期,集資淨額將主要用作,臨床開發和推進其他臨床階段藥物。
上市申請文件又提及, 公司是一家位於中國,處於商業化階段的創新型生物製藥公司,研發創新平台由超過420名科學家及員工的團隊所組成,專注於全球創新及中國癌症市場。
和黃中國醫藥科技在2000年由和記黃埔成立,致力於開發治療癌症汞自身免疫疾病的新藥,過往曾與默克、阿斯利康及廣東白雲山等大型藥企合作。其中,公司有一款用於治療轉移性大腸癌的藥物,去年獲批在中國上市及銷售。
5 : GS(14)@2019-04-18 07:49:30
http://www.takungpao.com.hk/231106/2019/0416/276481.html
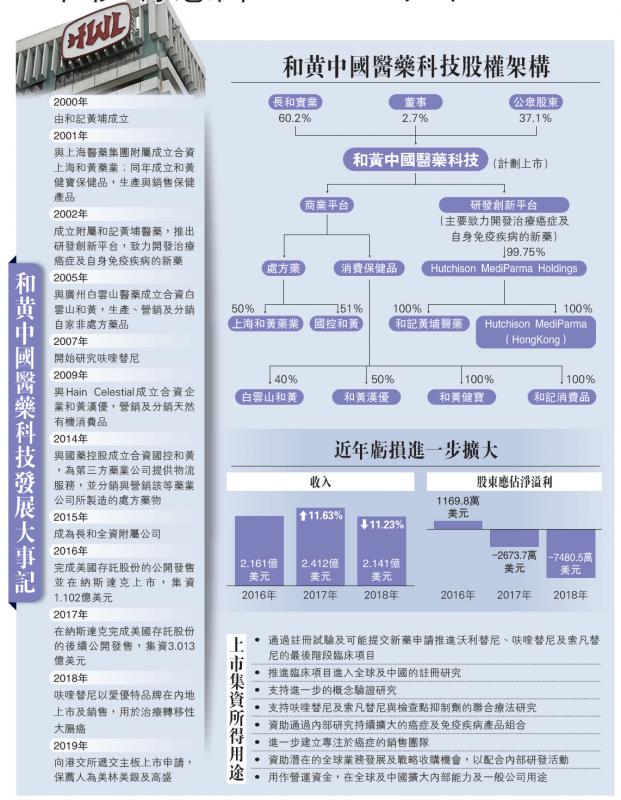
長和(00001)持股60.2%的和黃中國醫藥科技,向港交所(00388)遞交主板上市申請。根據初步招股文件,和黃中國醫藥科技去年股東應佔虧損進一步擴大至7480.5萬美元(約5.8億港元),而長和有意在上市後將持股降至50%以下,其業績不再於長和財務報表合併入帳。外電引述消息指,該公司計劃集資5億美元(約39億港元),目標在第三季完成。若成功分拆上市,將是2015年長實與和黃「世紀大重組」後,最大一宗商業決定。\大公報記者 林靜文
成立於2000年的和黃中國醫藥科技,是一家處於商業化階段的創新型生物製藥公司,擁有商業及研發創新兩大業務,前者專注於全球創新及中國癌症市場。目前有八種正在進行臨床試驗的自主研發候選藥品,當中五種已或將要開始全球臨床開發。後者主要銷售處方藥及消費保健品。
去年虧損5.8億
和黃中國醫藥科技於2006年在倫敦證券交易所的AIM(另類投資市場)上市,2016年其美國存託股份在納斯達克上市。港交所去年修改上市條例,未盈利的生物科技股亦可來港上市。
和黃中國醫藥科技主席杜志強表示,中國生物科技生態系統發展迅速,而近期的政策改革亦加快了創新藥物的審批時間,加上港交所放寬生物科技企業來港上市,有助相關企業獲取資金。他預計,在港上市可為現時在納斯達克及倫敦AIM上市帶來補充,同時增長流動性及強化資金渠道,加強藥品研發能力,助力集團成為國際性的生物製藥企業。
文件顯示,和黃中國醫藥科技2018財年收入同比減少11.2%,主要是由於處方藥業務因內地實施「兩票制」,令收入減少所致,預計2019財年有關業務將進一步受到影響。在2016財年至2018財年期間,和黃中國醫藥科技僅2016年錄得純利1169.8萬美元,其後兩年分別虧損2673.7萬美元和7480.5萬美元。
和黃中國醫藥科技表示,未來的盈利能力主要取決於候選藥物商業化是否能夠成功。迄今,去年11月推出的呋喹替尼,是集團唯一獲得批准銷售的候選藥物,主要用於治療三線轉移性結直腸癌患者。至於其他候選藥物仍在開發階段,若過程遇到嚴重延誤,對業務會帶來重大損害。
和黃中國醫藥科技行政總裁Christian Hogg表示,視乎臨床結果,目標未來兩年沃利替尼和索凡替尼可獲批准,鞏固集團作為中國腫瘤學領先者的地位。
霍建寧:維持重大投資
對於長和有意將持股降至50%以下,有指其看淡業務前景,及因研發投入大而帶來風險。惟有消息稱,長和是次減持是為配合招股所需。長和董事總經理霍建寧在新聞稿中也指出,為更大限度地提升患者利益和股東價值,需要為和黃中國醫藥科技提供充分的靈活性,以加快其對自身戰略目標的投資。他強調,和黃中國醫藥科技具強勁的增長潛力,並計劃繼續維持在其的重大持股作為長期投資。
據介紹,是次集資所得,集團將用於通過註冊試驗及可能提交新藥申請推進沃利替尼、呋喹替尼及索凡替尼的最後階段臨床項目;推進臨床項目進入全球及中國的註冊研究;支持進一步的概念驗證研究;支持呋喹替尼及索凡替尼與檢查點抑制劑的聯合療法研究等。是次在港上市的聯席保薦人為美銀美林及高盛。
6 : GS(14)@2019-04-18 07:49:43
http://hk.bbwc.cn/g2pkw4.html
和黃中國醫藥在倫敦大漲,因癌症新葯研製取得積極進展
中國生物科技行業投資規模高達數十億美元,但鮮有世界級的藥物誕生
“我們如今的成就證明,公司作為創新生物製藥公司已經在中國立穩腳跟”
億萬富豪李嘉誠支援的和黃中國醫藥科技有限公司表示,在結直腸癌藥物的後期研製階段取得積極進展,公司向擁有針對此類疾病的自主研製藥物目標又跨出了一步。
3月3日,總部在香港的和黃中國醫藥科技釋出聲明稱,目前正準備向中國國家食品藥品監督管理總局遞交呋喹替尼(Fruquintinib)的新葯申請。當地時間10:26,公司股價在倫敦大幅上漲9.6%,報22.875英鎊。
和黃中國醫藥的發展顯示,中國生物科技企業正在推進創新藥物的開發,而此類藥物的售價往往高於通用名仿製藥。雖然過去十年,中國生物科技行業投資規模高達數十億美元,但鮮有世界級的藥物誕生。和黃中國醫藥目前取得的進展暗示,其有望在中國和全球市場實現該藥物的商業化,同時也讓投資者獲得更加明確的回報前景。
公司執行長賀雋表示,“我們如今的成就證明,公司作為創新生物製藥公司已經在中國立穩腳跟。我們花了17年的時間走到今天:對公司而言,是一個重要的里程碑。”
和黃中國醫藥成立於2000年,主要股東是長和。賀雋是其第一個僱員,2000年到2005年期間,李嘉誠旗下集團向其注資超過7500萬美元。
和黃中國醫藥在聲明中表示,其呋喹替尼療法實現了提高病患總體存活率的主要目標。公司也在納斯達克上市,訊息公佈時,該市場尚未開始交易。撰文/Natasha Khan 編輯/劉馨蔚
總之 總部在香港的和黃中國醫藥科技釋出聲明稱,在結直腸癌藥物的後期研製階段取得積極進展。
7 : GS(14)@2019-04-18 07:50:33
http://www.hkexnews.hk/app/SEHK/ ... ls-2019041501_c.htm
招股書
8 : GS(14)@2019-04-18 07:50:47
[realblog]https://realblog.zkiz.com/greatsoup38/22538[/realblog]
9 : 太平天下(1234)@2019-04-18 10:17:58
greatsoup在7樓提及
http://www.hkexnews.hk/app/SEHK/2019/2019041501/SEHKCaseDetails-2019041501_c.htm
招股書
和黃牌頭的, 不過老股民應該有陰影吧
10 : GS(14)@2019-04-22 16:56:31
不要了
PermaLink: https://articles.zkiz.com/?id=352511
Next Page